ملخص الوحدة الثانية العلاقة بين بنية و وظيفة البروتين مع باقة متنوعة من التمارين للسنة الثالثة ثانوي شعبة علوم تجريبية و رياضيات 2025/2026
مرحباً بتلاميذ السنة الثالثة ثانوي شعبتي العلوم التجريبية والرياضيات! نقدم لكم هذا المورد التعليمي المتكامل حول الوحدة الثانية “العلاقة بين بنية البروتين ووظيفته”، وهو مصمم خصيصاً ليتوافق مع منهاج بكالوريا 2026. يهدف هذا الملخص إلى تبسيط المفاهيم المعقدة وتقديمها بطريقة منهجية تساعدكم على الاستيعاب العميق والتحضير الأمثل للامتحانات.
تعتبر البروتينات جزيئات حيوية أساسية تلعب أدواراً محورية في جميع العمليات الحيوية داخل الكائن الحي. فهم العلاقة الدقيقة بين بنيتها الفراغية المعقدة ووظيفتها المتخصصة هو مفتاح النجاح في مادة علوم الطبيعة والحياة. من خلال هذا الدرس، سنغوص في عالم الأحماض الأمينية، ونكتشف كيفية ارتباطها لتشكيل سلاسل بيبتيدية، ثم نرى كيف تتخذ هذه السلاسل بنيات ثلاثية الأبعاد تحدد تخصصها الوظيفي بدقة.
🔬 العلاقة بين بنية ووظيفة البروتين
يأخذ البروتين بعد تركيبه على مستوى الريبوزومات بنية فراغية معقدة ومميزة تحدد خصوصيته الوظيفية عن باقي البروتينات. تقوم البروتينات بالعديد من الوظائف الحيوية المتنوعة؛ فهي تدخل كمادة بنائية لجسم الكائن الحي، كما تعمل كمادة متخصصة وظيفياً كتنشيط التفاعلات الحيوية (الإنزيمات)، وتنظيم العمليات الحيوية في الخلية والجسم (الهرمونات)، وكوسائل دفاعية (الأجسام المضادة). ويعود هذا التخصص الوظيفي للبروتينات إلى البنية الفراغية التي تتميز بها هذه الجزيئات.
1. الأحماض الأمينية
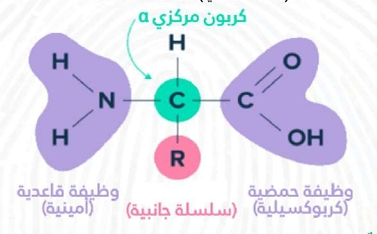
هي جزيئات بسيطة تمثل الوحدة البنائية الأساسية للبروتينات، وهي مركبات عضوية مقسمة إلى جزأين:
- الجزء الثابت: يحتوي على مجموعة كربوكسيلية (حمضية COOH-) ومجموعة أمينية (قاعدية NH2-) متصلتين بذرة كربون α.
- الجزء المتغير: يتمثل في سلسلة جانبية (جذر ألكيلي) يرمز له بـ R، يختلف تركيبه من حمض أميني لآخر.
تصنيف الأحماض الأمينية:
تصنف الأحماض الأمينية حسب السلسلة الجانبية (الجذر R) إلى:
- أحماض أمينية قاعدية: وفيها يحتوي الجذر R على وظيفة قاعدية وهي: ليزين (Lys)، أرجينين (Arg) وهيستدين (His).
- أحماض أمينية حمضية: وفيها يحتوي الجذر R على وظيفة حمضية وهي: حمض غلوتاميك (Glu) وحمض أسبارتيك (Asp).
- أحماض أمينية متعادلة: وفيها لا يحتوي الجذر R على وظيفة حمضية أو قاعدية وهي: بقية الأحماض الأمينية (عددها 15). يمكن تقسيمها حسب نوع الوظائف الموجودة في جذورها إلى: كحولية، عطرية، كبريتية، أليفاتية، أميدية، حلقية.
الخاصية الأمفوتيرية (الحمقلية):
يتميز الحمض الأميني بالخاصية الأمفوتيرية أو الحمقلية لأنه يحمل وظيفتين قابلتين للتأين (حمضية و قاعدية)، مما يجعله يسلك سلوك الحمض في الوسط القاعدي (يحرر بروتون H+)، وسلوك القاعدة في الوسط الحامضي (يكسب بروتوناً). لذلك تسمى بالمركبات الأمفوتيرية.
يتميز كل حمض أميني بنقطة تعادل كهربائي (pHi) خاصة به وتختلف عن الأحماض الأخرى وهي درجة الـ pH التي يكون فيها الحمض متعادل كهربائياً (عدد الشحنات الموجبة والسالبة متساوٍ، أي شحنة معدومة).
- عند pH = pHi: شحنة الحمض الأميني معدومة. يسلك سلوك حمض وقاعدة في نفس الوقت.
- عند pH < pHi: شحنة الحمض الأميني موجبة. الوسط حامضي، يسلك الحمض الأميني سلوك قاعدة ويكتسب بروتوناً.
- عند pH > pHi: شحنة الحمض الأميني سالبة. الوسط قاعدي، يسلك الحمض الأميني سلوك حمض ويحرر بروتوناً.

الصيغة الكيميائية للأحماض الأمينية في درجات pH مختلفة:
https://iili.io/KbNUsR9.png🔗 الرابطة البيبتيدية والبنية الفراغية للبروتين
الرابطة البيبتيدية:
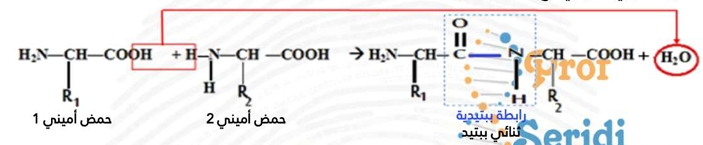
تتحد الأحماض الأمينية مع بعضها البعض مشكلة سلاسل بيبتيدية تُعطي في مجموعها البروتينات. ترتبط الأحماض الأمينية المتتالية في سلسلة بيبتيدية بروابط تكافؤية تدعى الرابطة البيبتيدية (-CO-NH-) والتي تتشكل نتيجة ارتباط الوظيفة الكربوكسيلية (-COOH) للحمض الأميني الأول مع الوظيفة الأمينية (-NH2) للحمض الأميني الموالي مع انطلاق جزيئة ماء.
البنية الفراغية للبروتين:
يمكن تمثيل البنية الفراغية للبروتين بعدة نماذج أهمها:
- نموذج الكرة والعود (Batonnets et Boules): يهدف إلى إظهار الذرات والروابط الموجودة فيما بينها.
- نموذج الكرة أو المكدس (Sphères): إظهار حجم الجزيئة وتظهر الذرات فقط.
- نموذج العود (Batonnets): إظهار الروابط الكيميائية في الجزيئة.
- النموذج الشريطي (Rubans): يسمح بتوضيح البنيات الثانوية للجزيئة (الحلزونية α والوريقية β) ومناطق الانعطاف.
المستويات البنيوية للبروتين:
يمكن تقسيم المستويات البنيوية للبروتينات حسب درجة التعقيد إلى 4 مستويات:
- البنية الأولية: هي تتابع الأحماض الأمينية المرتبطة فيما بينها بروابط بيبتيدية (تكافؤية قوية) فقط لتكوين سلسلة بيبتيدية.
- البنية الثانوية: هي التفاف (انطواء) السلسلة البيبتيدية ذات البنية الأولية في مناطق محددة وذلك بتشكيل روابط هيدروجينية. نميز فيها نوعين: البنية الحلزونية α والبنية الوريقية β.
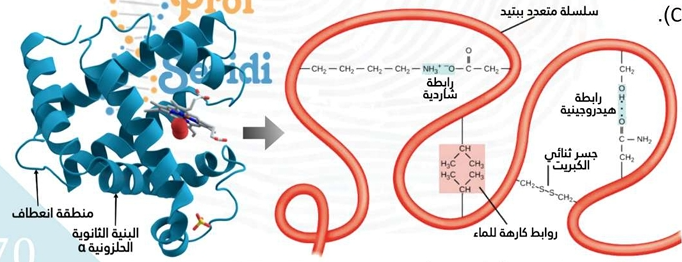
- البنية الثالثية: هي انطواء السلسلة البيبتيدية ذات البنية الثانوية على مستوى المناطق البينية. تُحافظ على استقرارها بوجود أربعة أنواع من الروابط: هيدروجينية، شاردية، تجاذب الجذور الكارهة للماء، والجسور ثنائية الكبريت (تكافؤية قوية).
- البنية الرابعية: هي تجمع لسلسلتين بيبتIDيتين أو أكثر لكل منها بنية ثالثية وتسمى كل سلسلة بتحت وحدة. ترتبط تحت الوحدات بروابط ضعيفة (هيدروجينية، شاردية، كارهة للماء).
العلاقة بين بنية ووظيفة البروتين
تحدد المعلومات الوراثية عدد ونوع وترتيب الأحماض الأمينية المركبة للبروتين. تنشأ بين هذه الأحماض الأمينية روابط في مواضع محددة (هيدروجينية، ثنائية الكبريت، شاردية، وتجاذب الجذور الكارهة للماء)، فتنتج بنية ثابتة ومستقرة للبروتين تحدد وظيفته وبالتالي التخصص الوظيفي للبروتين.
في حالة تغير في الأحماض الأمينية أو تفكيك الروابط المحافظة على استقرار البنية بتدخل عوامل فيزيائية أو كيميائية، يؤدي ذلك إلى تخريب بنيته الفراغية وبالتالي فقدان تخصصه الوظيفي. قد يكون التخريب عكسياً (يمكن استرجاع البنية والوظيفة) أو غير عكسي (لا يمكن استرجاع البنية والوظيفة).
تجربة Anfinsen:
أوضحت تجربة أنفنسن على إنزيم الريبونيوكلياز أن البنية الفراغية للبروتين (وبالتالي وظيفته) تتحدد بالبنية الأولية (تتابع الأحماض الأمينية). عند معاملة الإنزيم بمواد تخرب الروابط (اليوريا ومركب B-مركبتوإيثانول)، يفقد بنيته ويصبح غير فعال. وعند إزالة هذه المواد، يستعيد الإنزيم بنيته الطبيعية ووظيفته تلقائياً، مما يدل على أن المعلومات اللازمة للانطواء الصحيح موجودة في التسلسل الأولي للأحماض الأمينية.
📥 تحميل ملخص الوحدة الثانية وتمارينها PDF
احصل على النسخة الكاملة من الملخص والتمارين بصيغة PDF للتحضير الشامل والمراجعة المركزة قبل الامتحانات.
تحميل الملف الآن📝 تمارين الوحدة الثانية مع الحلول
تمرين 01: تأثير الثوم على بكتيريا ARN بوليميراز
الثوم من أكثر الأغذية استعمالاً لما له من أهمية في علاج الكثير من الأمراض، وهذا لاحتوائه على مادة allicine التي تقضي على البكتيريا. الوثيقة التالية تمثل بنية إحدى تحت وحدات إنزيم ARN بوليمراز في غياب ووجود مادة allicine.
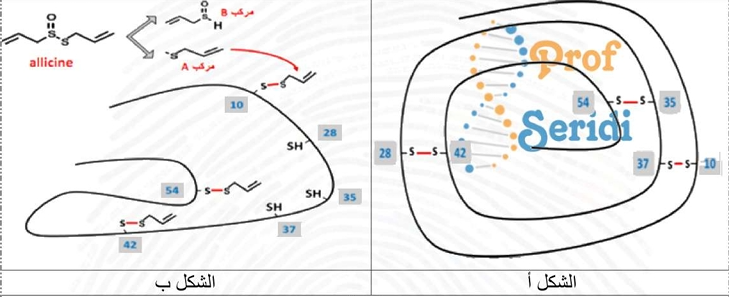
- اكتب صيغة الحمضين الأمينيين 10 و 37 إذا علمت أن الجذر هو CH2-SH.
- بين في نص علمي آلية تأثير الثوم في القضاء على البكتيريا اعتماداً على الوثيقة وعلى مكتسباتك.
تمرين 02: استقرار البنية الفراغية للبروتين
يُؤَمِّنُ استقرار التسلسل النيكليوتيدي في المورثات استقرار البنية الفراغية للبروتين ووظيفته إلا أنَّ بعض الاختلالات التي تصيب المورثة تُفقد البروتين تخصصه الوظيفي.
1. اختر العبارة الصحيحة من العبارات المقترحة لتكملة الجمل التالية:
- أ- الروابط التكافئية التي تساهم في استقرار البنية الفراغية للبروتينات هي: (الجسور ثنائية الكبريت / الروابط الكارهة للماء / الروابط الشاردية).
- ب- تتوقف البنية الفراغية وبالتالي التخصص الوظيفي للبروتينات على: (الروابط التي تنشأ بين أحماض أمينية محددة / طبيعة وعدد الأحماض الأمينية فقط / عدد وترتيب الأحماض الأمينية فقط).
- ج- إن ترتيب الأحماض الأمينية في السلسلة الببتيدية يفرضه ترتيب الرامزات في: (ARNr / ARNm / ARNt).
- د- أصل الطفرة الوراثية هو تغير على مستوى: (ARNm / ADN / البروتين).
2. وضح في نص علمي كيف يحافظ التسلسل النيكليوتيدي للمورثة على وظيفة البروتين مبرزاً دور بعض الطفرات في فقدان التخصص الوظيفي.
تمرين 03: مرض التلاسيميا (فقر الدم)
مرض التلاسيميا هو عجز في إمداد الأكسجين للجسم ناتج عن استبدال نيكليوتيدة T بـ C على مستوى مورثة التحت وحدة α1 للهيموغلوبين. الشكل (أ) يمثل مرحلة بداية ترجمة التحت وحدة α1 عند شخص سليم. الشكل (ب) يعرض البنية الفراغية للهيموغلوبين.
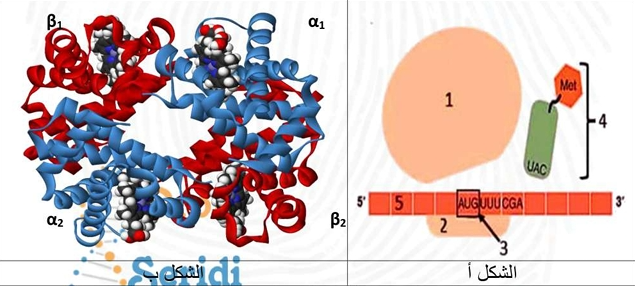
- تعرف على البيانات المرقمة في الشكل (أ) والمستوى البنائي للهيموغلوبين المبين في الشكل (ب).
- بيّن في نص علمي كيف أثر تغير نيكليوتيدة واحدة من مورثة الهيموغلوبين في مرض التلاسيميا على بنية الهيموغلوبين.
🤔 أسئلة شائعة حول بنية ووظيفة البروتين
ما هي العلاقة الأساسية بين بنية البروتين ووظيفته؟
العلاقة بين بنية البروتين ووظيفته هي علاقة تحديد وتخصص. البنية الفراغية ثلاثية الأبعاد للبروتين، التي تنتج عن تتابع ونوع الأحماض الأمينية (البنية الأولية) وطريقة انطوائها، هي التي تحدد شكله النهائي ومواقعه النشطة. هذا الشكل الدقيق هو الذي يسمح للبروتين بأداء وظيفته الخاصة، مثل الارتباط بركيزة معينة (إنزيم) أو نقل جزيء محدد (هيموغلوبين).
كيف تتشكل الرابطة البيبتيدية بين الأحماض الأمينية؟
تتشكل الرابطة البيبتيدية من خلال تفاعل نزع للماء (تكاثف) بين حمضين أمينيين. يتم التفاعل بين مجموعة الكربوكسيل (-COOH) لحمض أميني ومجموعة الأمين (-NH2) للحمض الأميني التالي. ينتج عن هذا التفاعل إزالة جزيء ماء (H2O) وتكوين رابطة تكافؤية قوية بين ذرة الكربون من مجموعة الكربوكسيل وذرة النيتروجين من مجموعة الأمين، وتعرف هذه الرابطة بـ (-CO-NH-).
متى يفقد البروتين بنيته الفراغية الطبيعية؟
يفقد البروتين بنيته الفراغية الطبيعية، في عملية تسمى “التخريب” أو “Denaturation”، عند تعرضه لظروف قاسية تغير من استقراره. تشمل هذه الظروف التغيرات الكبيرة في درجة الحرارة (الحرارة العالية)، التغيرات الشديدة في درجة الحموضة (pH)، أو وجود مواد كيميائية معينة مثل اليوريا. هذه العوامل تكسر الروابط الضعيفة (كالهيدروجينية والشاردية) التي تحافظ على البنية الثالثية والرابعية.
أين تكمن أهمية تجربة أنفنسن في فهم وظيفة البروتين؟
تكمن أهمية تجربة أنفنسن في أنها أثبتت بشكل قاطع أن المعلومات الضرورية والكافية لتحديد البنية الفراغية الصحيحة للبروتين (وبالتالي وظيفته) محمولة بالكامل ضمن تسلسل الأحماض الأمينية (البنية الأولية). هذا يعني أن عملية انطواء البروتين ليست عشوائية، بل هي عملية موجهة ذاتياً بناءً على الشفرة الوراثية التي تحدد هذا التسلسل.
لماذا تعتبر الأحماض الأمينية مركبات أمفوتيرية (حمقلية)؟
تعتبر الأحماض الأمينية مركبات أمفوتيرية أو حمقلية لأنها تحتوي في بنيتها على وظيفتين كيميائيتين متعاكستين: وظيفة حمضية (مجموعة الكربوكسيل -COOH) ووظيفة قاعدية (مجموعة الأمين -NH2). هذه الطبيعة المزدوجة تجعلها قادرة على التصرف كحمض (بفقدان بروتون) في وسط قاعدي، وكقاعدة (باكتساب بروتون) في وسط حامضي.
لمن يوجه هذا الملخص والتمارين؟
هذا المورد التعليمي موجه بشكل أساسي لتلاميذ السنة الثالثة ثانوي في الجزائر، لشعبتي العلوم التجريبية والرياضيات، الذين يدرسون مادة علوم الطبيعة والحياة ضمن منهاج بكالوريا 2026. كما أنه مفيد جداً للأساتذة كمصدر للمراجعة وإعداد التمارين، ولأولياء الأمور الراغبين في متابعة أبنائهم ودعمهم في التحضير للامتحانات.




